INTERVIEW
知財インタビュー
2020.10.05
知財インタビュー
Vol.4
核酸医薬分野における産学官の連携とバイオベンチャーの設立

脳神経病態学分野の横田隆徳先生。多くの知財を取得し、第3の核酸医薬として注目される「ヘテロ核酸」を軸に、神経難病治療薬の開発に向けてベンチャー企業も設立されています。研究のパートナーとの出会いや、企業とのコラボレーションなどについてうかがいました。
- プロフィール
-
医歯学総合研究科
脳神経病学分野
教授
横田隆徳先生
研究について
先生はアカデミアや製薬会社とのコラボレーションに積極的に取り組まれ、治療薬の実現を目指されています。「ヘテロ核酸」の研究に取り組んだきっかけや目指していること、研究の面白いところを教えてください。
- 横田:
- 私は脳神経内科医で、大学院医歯学総合研究科の脳神経病態学分野の教授をしています。内科の中で神経系の疾患を診療していますが、患者さんが多いのは、脳梗塞や脳出血などの脳卒中、アルツハイマー病などの認知症、てんかん、頭痛ですが、さらには、脳炎、髄膜炎など感染症、ギランバレーなどの末梢神経障害、筋ジストロフィーなどの筋疾患など、幅広いです。
脳の神経系の疾患には、アルツハイマー病などの神経難病で、なかなか治らないものが多くあります。長い間とても苦しまれて亡くなる方を見てきているので、神経難病の治療薬を作ろうと模索してきました。しかし、私が医師になったばかりの頃は、神経難病のメカニズムがほとんど分からない状況で、治療するにも取っ掛かりがありませんでした。神経難病のメカニズムが分かってきたのはこの10年くらいのことです。それでも、現時点で遺伝性の神経難病の多くの原因遺伝子が見つかって、その発症メカニズムも概ね50%くらい解明されてきたという印象です。
先生は医師なので、「創薬」からは離れた立ち位置だと思いますが、それが実現できた経緯を教えてください。
- 横田:
- 私自身も、自分で新しい薬を作るという発想は全くありませんでした。創薬は化学者だったり薬学者だったり、製薬会社のお仕事であり、医師である私たちはそれを応用したり、その手前のメカニズムを研究するのが役目だと思っていましたから。
でも、2000年に留学から帰ってきて、当時分かっていた神経難病のメカニズムは全体の10%位でしたが、「その10%で治療をすればいいのでは?」と考え、治療研究を専門の1つにしました。既存の核酸医薬、主にsiRNA(RNA干渉)だったんですが、その応用研究を行っていました。まだ核酸医薬が現実の薬になるかどうかについて、多くの人が懐疑的だった時代です。そこで、既に分かっている標的に対して製薬会社が作ったsiRNAを応用し、サルで実験などもしていましたが、なかなかこの方法で「治る」という確信が持てるところまでは進められなかったのです。論文は書けても毎日診ている目の前の患者さんを本当に治せる実感が乏しくて、悔しい思いをしていました。当時は40代でしたが、これをずっと続けていいのかなと、鬱々としていた時期がありました。
そんな矢先、さらにショッキングなことが起こりました。siRNAによるRNA干渉について研究しているアルナイラムというバイオ企業があり、ファイザーや武田薬品などのメガファーマが一緒に創薬開発をしていました。そのファイザーや武田薬品が、2013~2015年頃にsiRNA開発からの撤退を発表したのです。メガファーマのトップがsiRNA分野をあきらめたということは、治療薬としての見込みがないという結論を下したということ。当時は大阪大学で先進的な化学修飾核酸を研究している小比賀聡先生と共同研究をしていて、私もアンチセンス核酸をやろうと思っていたタイミングでした。しかし、論文は書けても患者を治せないのなら意味がない。「自分の研究も止めるべきなのか?」、そう考えました。
その時は、アンチセンス核酸にしてもsiRNAにしても、私は既存のものを使っていました。しかし一応私も科学者の端くれです。人のものを使って研究するのはやめて、自分で考えてみようと決心しました。そこで、小比賀聡先生に相談するために大阪へ向かう飛行機の中で思いついたのが「ヘテロ核酸」だったのです。その日は小比賀先生と分子構造を議論して、あっという間に夜中になって大阪に泊まったことを覚えています(笑)。当初はその有効性に半信半疑でしたが、動物実験をしてみたら、これがもの凄く効いて自分でもびっくりしました。
ヘテロ核酸とアンチセンス核酸との一番の違いは何ですか。
- 横田:
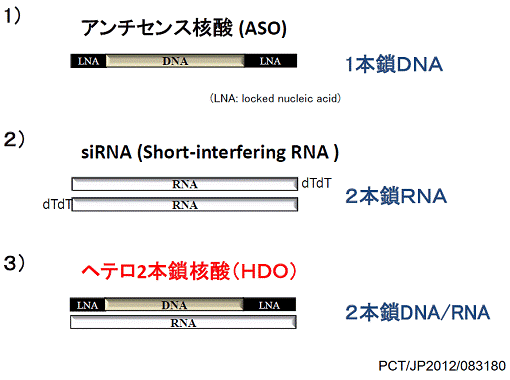
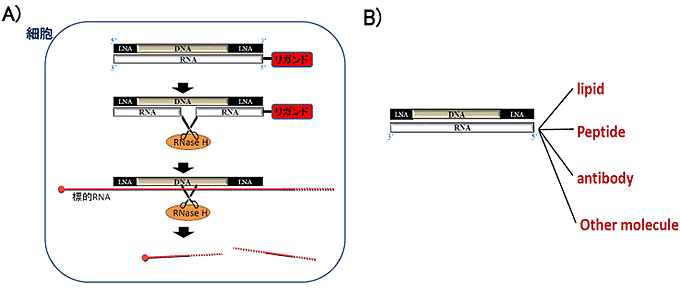
- ヘテロ核酸のもともとの発想は、アンチセンス核酸にデリバリー分子(リガンド)を結合させた応用版なんです。ヘテロ核酸はアンチセンス核酸のDNAとRNA相補鎖の組み合わせなのですが、RNA相補鎖にはリンカーを介して様々なリガンドを結合することができます。
しかし「それだけではないな」と思ったのは、細胞内でのヘテロ核酸(DNA/RNA)の高次構造がアンチセンス核酸(1本鎖DNA)やsiRNA(2本鎖RNA)と大きく異なり、細胞内で生物学的に固有の認識をされて、独自のトラフィッキング経路を持っていることが判明したからです。そして、リガンドの結合が無くてもヘテロ核酸はアンチセンス核酸より効果が強いため、ヘテロ核酸を第3の核酸医薬と考えるに至りました。アンチセンス核酸の単なる応用ではないという学問的な知見から、今までとは異なる別のモダリティの核酸医薬ということで、多くの化学者や製薬会社の方から注目されたのだと思います。
研究のパートナーと学内のサポート
先生同士のつながりで誕生した研究とのことですが、さらに研究を進めるに当たってどのような協力があったのでしょうか。
- 横田:
- 小比賀先生と出会う前から一緒に研究させていただいているのが東京理科大学の和田猛先生です。和田先生は純粋な化学者ですが、発想が斬新で面白いし、性格が非常に明るくて一緒にいて楽しい方です。
印象に残っているのは、ある土曜日の午後に私の携帯電話に着信が入り、誰かと思うと和田先生です。「横田先生、面白いこと思い付いちゃいました!今からうかがってもいいですか?」と。私は自宅に帰って子供と食事しようというタイミングでしたが、すぐ来てもらいました。和田先生は熱心に説明してくださったのですが、そのときは正直その価値がよく分かりませんでした(笑)。実はそれは後に素晴らしい発明になってヘテロ核酸にも応用しています。
小比賀先生と和田先生の3人で会うようになったのは、CRESTという文部科学省のJST(科学技術振興機構)のグラント(研究費)が採用されたときからで、そこからほぼ定期的にミーティングをしています。私は疾患を治療可能な人工分子の設計をしてお二人に提案して合成してもらっていますし、一方、お二人の発明した新規の人工核酸や化学修飾を、患者さんの役に立つ核酸医薬の分子構造にするのが私の役割です。私は患者さんの役に立つためにはどういうニーズがあるのか、どういうプロパティが必要なのかをお二人に伝える。彼らは私の伝えたニーズに合わせたものを作ってくれる。そういうキャッチボールを、3人の間でできるようになりました。
知的財産や技術の権利をしっかりと守りながら、使ってもらえるパートナーと組めるかどうかは、学内の体制も重要ですね。
- 横田:
- 私が最初に特許を申請したのは2004年で、C型肝炎ウイルスRNAの複製抑制siRNAでした。当時、まずは総務課に相談するように言われて行ってみると、総務課では「この人に相談して下さい」と、弁理士の名刺を渡されておしまいでした。ヘテロ核酸の時は知財部ができていましたが、当時の医学部長の湯浅先生に大変なご支援をいただいきました。多額の投資によって米国の弁理士をつけていただいて、特許の補強をして頂いたことは現在の成果に大きく貢献しました。
現在のオープンイノベーション機構や産学連携研究センターには、知財、ビジネスの専門家が急速に整備、組織されて、ヘテロ核酸関連の20を超える特許の知財戦略にお世話になっており大変感謝しております。
ベンチャー立ち上げとパートナー企業
先生は「レナセラピューティクス」というベンチャー企業の立ち上げをされましたが、どのように実現されたのでしょうか。
- 横田:
- 「レナセラピューティクス」は、「ヘテロ核酸」という新しい核酸医薬品の創製を目的とした本学発のバイオベンチャー企業です。設立は大学の執行部の強力な主導によって、経済産業省の外郭団体である産業革新機構の出資よって実現しました。設立にあたっては、産学連携センターのお世話によって、テックマネージという技術移転会社のサポートを受けられたことも助かりました。
一般的には、研究者が国から助成を受けて、最終的に製薬会社などと組む形でしたが、今回の場合はシーズの段階から産業界が入って、国がそれを後押しするという流れだったということですね。
- 横田:
- アカデミア発でも社会や企業から評価を受けているところに対して投資が来るという良い循環になりました。期せずしてこうなったのは、企業との共同研究があったことと、ベンチャー企業が設立できたことが大きいですね。さらに国が良い形でサポートしてくれて今に至っていますが、健全な流れだと思います。
国のサポート
先生は多くの大型グラントに採択されていますね。
- 横田:
- 私の技術がここまで来られたもう1つのサポートは、国の大型グラントの後押しがありました。最初のJST CRESTグラントは、ホスホロチオエート基 (PS)を立体制御したヘテロ核酸が開発テーマでしたが、和田先生のPSキラル核酸技術も私のヘテロ核酸も論文はゼロでしたが、当時審査委員長だったシカゴ大学教授の山本尚先生というノーベル化学賞候補の先生が、特許の内容のみで選んで下さったのです。その後立て続けにAMEDから3つの数億円の大型グラントをいただけました。このように、ヘテロ核酸は大学と国の支援によって発展してきましたので、大変感謝しています。
オープンイノベーションの取り組み
先生が取り組まれている領域で、現状の薬の満足度と治療への貢献度は、どのぐらいになりますか。
- 横田:
- アンメット・メディカル・ニーズでは最も悪いですね。アルツハイマー病が代表的ですが、薬がないし、治療の選択肢がないですから。ただ、アプローチの道筋は少しずつできてきていると感じています。
製薬会社のサイエンティストと一緒に創薬研究を進めることは、アカデミアのサイエンティストとしてメリットは非常に大きいです。しかし、アカデミアの多くの研究者はそのことにまだ気付いてないと思います。企業と協力関係を構築しようというアカデミアの認識も足りませんし、企業側も目の前にあるマイルストーンばかり追いがちなので。早期のシーズを長期的に一緒に育てる余裕がないのが実情かもしれません。
そのよう中で、「大学と一緒に開発していく」という意思が垣間見えるのは、いくつかの製薬会社が企画しているアイデア提案型の共同研究です。オープンイノベーションの考え方が企業と大学双方に出始めているのでは、と思います。
アカデミアが今後重視すべきことは、どのようなことでしょうか。
- 横田:
- 企業が私たち医学部のアカデミアに求めているのは、今までとは発想が異なるサイエンスや、臨床的なアイデアではないでしょうか。特に、新しい創薬分野を切り開けるオリジナリティの高い発想が重要です。小手先の応用研究ではなくて、今まで以上に独自性の高いサイエンスが重要になってくると思います。山中伸弥先生のiPS細胞や大隅良典先生のオートファジーといった新しい概念を作ったり、新しい原理原則を見つけたりといったことは、まさに独自性の高いサイエンスです。
ただ企業は、その発想やその成果を患者さんに届けるにどう持っていったら良いかが分からないので、その橋渡しが大事だと思います。どうしたらブレークスルーのテクノロジーが薬になるのか、どういうステップがあって何が求められるのかということを、自分がやるかどうかは別として、過程やニーズを知識として持っていることは必要だと思います。
さらに科学者は、知財があって、ビジネスがあって、レギュレーションがあることを知っておかなければなりません。成果の社会実装に向けて、少なくとも秘密保持や知的財産などのビジネスの基本的なことを知っておく必要があると思います。本学では産学連携センターの飯田香緒里先生が学部学生に対してそうした講義をされていると聞いており、すばらしいと思います。企業等との共同研究に必要な基礎知識を身につけた研究者を育成できるといいなと思います。
そうした知識は、オープンイノベーション機構の活動にも直結しますね。オープンイノベーション機構に求めることはありますか。
- 横田:
- 若い研究者にオープンイノベーションの裾野を広げることは重要だと思います。しかし、オープンイノベーションは「ビジネス」につながることで、必ず勝ち負けが出てきます。医科歯科の代表的な知財に対してきちんとした戦略を立てて、突出した発展を促し、「勝つ知財」にすることが最も重要だと思います。勝たないとあとが続きません。
そのためには「専門の人材」が重要です。知財の導出は科学者の本分ではありませんので、PhD(博士号)や MD(医師)でありながらMBA(経営学修士号)も持っているなど、サイエンスと知財とビジネスを広く理解できるエキスパート人材を育てることが大事だと思います。さらには、業界の一流のビジネスパーソンを適正な給与で雇用したり、あるいは適切な成功報酬を支払うことなども考える必要があると思います。
最後に先生のご趣味を聞かせて下さい。
- 横田:
- 週末には妻と皇居を走っています。私は元々サッカーをやっていたので、体を動かすことは好きです。ただ、新型コロナウイルスの影響で外出できなくなったので、自宅の庭で野菜を育てていて、最近、ナスだ、バジルだの収穫ができるようになって、これにはまっています。

ありがとうございました。
CONTACT
東京科学大学医療イノベーション機構に関するお問い合わせ、お申し込みは下記フォームにご入力ください。
